Sabtu, 30 Maret 2013
Kandidiasis
Kandidiasis, adalah infeksi spesies Candida, dengan Candida albicans sebagai penyebab yang paling banyak ditemui.[1]
Blastomikosis
Blastomikosis adalah penyakit menular yang disebabkan oleh cendawan dimorfik Blastomyces dermatitidis.[1] Cendawan B. dermatitidis banyak ditemukan di tanah yang mengandung sisa-sisa bahan organik dan kotoran hewan.[1] Ketika konidia (salah satu bagian tubuh) dari B. dermatitidis terhirup oleh manusia maka akan terjadi perubahan bentuk dari miselium menjadi khamir dan sistem imun manusia tidak sempat menghasilkan respon imun terhadap perubahan tersebut.[1] Agen penyakit akan menyebar melalui sistem limfa dan aliran darah.[1] Gejala penyakit ini sangat bervariasi karena banyak sistem organ yang berperan dalam penyebarannya.[1] Namun, beberapa gejala yang paling sering diperiksakan adalah gejala yang berkaitan dengan manifestasi pulmonari, lesi pada kulit yang tidak sembuh, lesi tulang yang seringkali tanpa rasa sakit, dan gejala yang berkaitan dengan sistem genitouorinari (urogenital).[1] Uji keberadaan infeksi dalam tubuh dapat dilakukan dengan biopsi jaringan tubuh untuk mengkultur dan melihat histopatologinya, mengambil sampel dari sekresi (pembuangan) sisa kotoran tubuh dan jaringan.[2]
Sistinosis
Sistinosis adalah penyakit dimana terjadi abnormalitas pada zat
cystine. Penyakit ini adalah yang sangat langka dan belum bisa diobati
sepenuhnya. Cysitinosis merupakan penyakit turunan, dimana cystine
diproduksi dalam sel-sel tubuh secara berlebihan. Jika tubuh kelebihan
cystine, sel-sel akan memadat karena cystin akan saling bergabung dan
membentuk kristal.
Sistinosis adalah penyakit dimana terjadi abnormalitas pada
zat cystine. Penyakit ini adalah yang sangat langka dan belum bisa
diobati sepenuhnya. Cysitinosis merupakan penyakit turunan, dimana
cystine diproduksi dalam sel-sel tubuh secara berlebihan. Jika tubuh
kelebihan cystine, sel-sel akan memadat karena cystin akan saling
bergabung dan membentuk kristal.
| Sistinosis | |
| Klasifikasi dan bahan-bahan eksternal | |
 |
|
|---|---|
| Chemical structure of cystine formed from L-cysteine (under biological conditions) | |
| ICD-10 | E72.0 |
| ICD-9 | 270.0 |
| DiseasesDB | 3382 |
| eMedicine | ped/538 |
| MeSH | D003554 |
Pranala luar
- Cystinosis - Cystinosis Research Foundation- an international research support and education foundation
- Cystinosis Research Network - a non-profit organization advocating research, providing family assistance, and educating the public about cystinosis.
- BC Health Guide
- Cystinosis Foundation UK - a UK Charity Supporting Families & Research
- Hide and Seek Foundation For Lysosomal Disease Research
| Artikel bertopik penyakit ini adalah sebuah rintisan. Anda dapat membantu Wikipedia dengan mengembangkannya. |
Porfiria
Porfiria berasal dari bahasa Yunani πορφύρα, porphura yang berarti "warna ungu". Hal ini merujuk pada warna urin pasien porphyria yang mengandungi warna menyebabkan warnanya berubah menjadi merah hingga biru gelap.
Porphyria bukan merupakan penyakit menular tetapi merupakan penyakit genetika yang diwaris dari orang tua.
Porphyria bukan merupakan penyakit menular tetapi merupakan penyakit genetika yang diwaris dari orang tua.
Mikrosefalus
Mikrosefalus adalah kelainan otak dengan ukuran kepala
lebih kecil dari ukuran kepala rata-rata berdasarkan umur dan jenis
kelamin. Kepala dikatakan lebih kecil jika ukuran lingkar kepala kurang
dari 42 cm atau lebih kecil dari standar deviasi 3 dibawah angka
rata-rata.
Mikrosefalus seringkali terjadi akibat kegagalan pertumbuhan otak pada kecepatan yang normal. Beberapa penyakit yang memengaruhi pertumbuhan otak dapat menyebabkan mikrosefalus. Mikrosefalus seringkali berhubungan dengan keterbelakangan mental. Mikrosefalus dapat terjadi setelah infeksi yang menyebabkan kerusakan pada otak pada bayi yang sangat muda (misalnya meningitis dan meningoensefalitis).
Mikrosefalus seringkali terjadi akibat kegagalan pertumbuhan otak pada kecepatan yang normal. Beberapa penyakit yang memengaruhi pertumbuhan otak dapat menyebabkan mikrosefalus. Mikrosefalus seringkali berhubungan dengan keterbelakangan mental. Mikrosefalus dapat terjadi setelah infeksi yang menyebabkan kerusakan pada otak pada bayi yang sangat muda (misalnya meningitis dan meningoensefalitis).
Fibrosis sistik
Fibrosis sistik atau fibrosis kistik (bahasa Inggris: cystic fibrosis, mucoviscidosis, CF) adalah radang akibat gangguan pada kanal klorida yang terletak pada lapisan epitelial.[1]
Penderita penyakit ini mengalami penumpukan fibrosis dan pembentukan kista pada kelenjar pankreas, saluran pernapasan dan pencernaan.[2] Penumpukan mukus menyebabkan bakteri lebih mudah berkembang biak sehingga infeksi bakteri, seperti pneumonia dapat terjadi.[2] Penyakit ini bersifat resesif, sehingga apabila kedua orang tua merupakan carier (pembawa) gen penyakit ini, maka satu dari empat anak mereka kemungkinan dapat menderita fibrosis sistik.[2] Penyakit ini timbul karena mutasi pada satu gen yang menyandikan protein pengatur perpindahan klorida dan natrium melalui selaput sel.[1] Akibatnya, terjadi dehidrasi dan pengentalan sekresi yang menyerang hampir seluruh kelenjar endokrin (kelenjar yang mengeluarkan cairan ke dalam saluran tertentu dalam tubuh).[1]
Kadar vitamin C yang rendah di dalam plasma darah maupun pada airway surface liquid ASL sering ditemukan pada fibrosis sistik, asma, chronic obstructive pulmonary disease, dan acute respiratory distress syndrome, perokok dan anak-anak yang terpapar asap rokok. Vitamin C memiliki peran yang unik pada cystic fibrosis transmembrane conductance regulator (CFTR).[3] Paparan asam askorbat, dengan senyawa peredam yaitu garam ekstraselular, merupakan stimulasi sekresi klorida transepitelial yang menyebabkan aliran mukus sepanjang permukaan ASL. Konsep ini didukung dengan fakta bahwa dosis vitamin C yang tinggi akan mengakibatkan diare, karena mukus yang berlebih.
Penderita penyakit ini mengalami penumpukan fibrosis dan pembentukan kista pada kelenjar pankreas, saluran pernapasan dan pencernaan.[2] Penumpukan mukus menyebabkan bakteri lebih mudah berkembang biak sehingga infeksi bakteri, seperti pneumonia dapat terjadi.[2] Penyakit ini bersifat resesif, sehingga apabila kedua orang tua merupakan carier (pembawa) gen penyakit ini, maka satu dari empat anak mereka kemungkinan dapat menderita fibrosis sistik.[2] Penyakit ini timbul karena mutasi pada satu gen yang menyandikan protein pengatur perpindahan klorida dan natrium melalui selaput sel.[1] Akibatnya, terjadi dehidrasi dan pengentalan sekresi yang menyerang hampir seluruh kelenjar endokrin (kelenjar yang mengeluarkan cairan ke dalam saluran tertentu dalam tubuh).[1]
Kadar vitamin C yang rendah di dalam plasma darah maupun pada airway surface liquid ASL sering ditemukan pada fibrosis sistik, asma, chronic obstructive pulmonary disease, dan acute respiratory distress syndrome, perokok dan anak-anak yang terpapar asap rokok. Vitamin C memiliki peran yang unik pada cystic fibrosis transmembrane conductance regulator (CFTR).[3] Paparan asam askorbat, dengan senyawa peredam yaitu garam ekstraselular, merupakan stimulasi sekresi klorida transepitelial yang menyebabkan aliran mukus sepanjang permukaan ASL. Konsep ini didukung dengan fakta bahwa dosis vitamin C yang tinggi akan mengakibatkan diare, karena mukus yang berlebih.
| Fibrosis sistik | |
| Klasifikasi dan bahan-bahan eksternal | |
 |
|
|---|---|
| Perawatan pernapasan pada penderita fibrosis sistik. | |
| ICD-10 | E84. |
| ICD-9 | 277.0 |
| OMIM | 219700 |
| DiseasesDB | 3347 |
| MedlinePlus | 000107 |
| eMedicine | ped/535 |
| MeSH | D003550 |
Fenilketonuria
Fenilketonuria (bahasa Inggris: Phenylketonuria, PKU) adalah gangguan desakan autosomal genetis yang dikenali dengan kurangnya enzim fenilalanin hidroksilase (PAH). Enzim ini sangat penting dalam mengubah asam amino fenilalanina menjadi asam amino tirosina. Jika tubuh kekurangan PAH, fenilalanina akan mengumpul dan berubah menjadi fenilketon, yang bisa dideteksi dari urin.
Jika dibiarkan, kondisi ini dapat menimbulkan masalah dalam perkembangan otak, menyebabkan fungsi mental menurun drastis dan serangan-serangan. Meski demikian, PKU merupakan salah satu dari sedikit penyakit genetis yang bisa dikendalikan melalui diet. Pasien yang diet rendah fenilalanina dan tinggi tirosina hampir dapat sembuh total.
Penderita tidak cocok memakan sesuatu yang mengandung fenilalanin.Seperti Permen Karet Doublemint. Salah satu contoh makanan yang mengandung fenilalanin adalah Garuda Kacang Atom[rujukan?]
Jika dibiarkan, kondisi ini dapat menimbulkan masalah dalam perkembangan otak, menyebabkan fungsi mental menurun drastis dan serangan-serangan. Meski demikian, PKU merupakan salah satu dari sedikit penyakit genetis yang bisa dikendalikan melalui diet. Pasien yang diet rendah fenilalanina dan tinggi tirosina hampir dapat sembuh total.
Penderita tidak cocok memakan sesuatu yang mengandung fenilalanin.Seperti Permen Karet Doublemint. Salah satu contoh makanan yang mengandung fenilalanin adalah Garuda Kacang Atom[rujukan?]
Defisiensi imunitas kombinasi
Defisiensi imunitas kombinasi (bahasa Inggris: Severe
combined immunodeficiency, SCID, Boy in the Bubble Syndrome,
Alymphocytosis, Glanzmann–Riniker syndrome, Severe mixed
immunodeficiency syndrome, Thymic alymphoplasia) adalah kelainan genetik yang menyebabkan bagian utama dari sistem kekebalan tiruan (Sel B dan Sel T) lumpuh, akibat berbagai kemungkinan yang disebabkan gen.
Pasien dengan penyakit ini mengalami kekurangan kekebalan. Penyakit ini
disebut juga dengan "bocah gelembung" karena pasien akan sangat rentan
terhadap penyakit infeksi.
Diare kronis, infeksi telinga, pneumonia, dan infeksi mulut umum muncul pada pasien ini. Jika gejala ini muncul pada bayi, biasanya bayi tersebut akan meninggal dalam waktu kurang dari 1 tahun akibat infeksi. Namun pilihan perawatan sudah berkembang pesat sejak kasus David Vetter.
Penyakit ini menyerang sekitar 1 dari 65 ribu kelahiran di Australia. Penelitian terbaru menunjukkan bahwa penyakit ini menyerang satu dari 2500 anak di Navajo.
Diare kronis, infeksi telinga, pneumonia, dan infeksi mulut umum muncul pada pasien ini. Jika gejala ini muncul pada bayi, biasanya bayi tersebut akan meninggal dalam waktu kurang dari 1 tahun akibat infeksi. Namun pilihan perawatan sudah berkembang pesat sejak kasus David Vetter.
Penyakit ini menyerang sekitar 1 dari 65 ribu kelahiran di Australia. Penelitian terbaru menunjukkan bahwa penyakit ini menyerang satu dari 2500 anak di Navajo.
Anemia sel sabit
Anemia sel sabit adalah kondisi serius di mana sel-sel darah merah menjadi berbentuk bulan sabit, seperti huruf C.
Sel darah merah normal berbentuk donat tanpa lubang (lingkaran, pipih
di bagian tengahnya), sehingga memungkinkan mereka melewati pembuluh darah dengan mudah dan memasok oksigen
bagi seluruh bagian tubuh. Sulit bagi sel darah merah berbentuk bulan
sabit untuk melewati pembuluh darah terutama di bagian pembuluh darah
yang menyempit, karena sel darah merah ini akan tersangkut dan akan
menimbulkan rasa sakit, infeksi serius, dan kerusakan organ tubuh.
Penyakit genetik
Penyakit genetik atau kelainan genetik adalah sebuah kondisi yang disebabkan oleh kelainan oleh satu atau lebih gen yang menyebabkan sebuah kondisi fenotipe klinis. Beberapa penyebab penyakit genetik antara lain:
- Ketidaknormalan jumlah kromosom seperti dalam sindrom Down (adanya ekstra kromosom 21) dan sindrom Klinefelter (laki-laki dengan 2 kromosom X).
- Mutasi gen berulang yang dapat menyebabkan sindrom X rapuh atau penyakit Huntington.
- Gen rusak yang diturunkan dari orang tua. Dalam kasus ini, penyakit genetik juga dikenal dengan istilah penyakit keturunan. Kondisi ini terjadi ketika individu lahir dari dua individu sehat pembawa gen rusak tersebut, tetapi dapat juga terjadi ketika gen yang rusak tersebut merupakan gen yang dominan.
Yersinia pestis
Yersinia pestis adalah bakteri Gram-negatif yang dapat tumbuh dengan atau tanpa oksigen (yang disebut kualitas tdk anaerobic).
Infeksi pada manusia mengambil tiga bentuk: pnumonik, septisemik, dan bubonik plak. Ketiga bentuk infeksi ini telah menyebabkan epidemik yang merenggut banyak korban dalah sejarah manusia, termasuk Plak Justinian pada 542 dan Kematian Hitam yang menyebabkan paling tidak mengambil sepertiga populasi Eropa dari 1347 sampai 1353. Belakangan ini, Y. Pestis juga dapat digunakan sebagai senjata biologi dan CDC telah mengklasifikasi bakteri ini ke dalam Patogen Kategori A sebagai persiapan serangan teroris.
Y. pestis ditemukan pada 1894 oleh Alexandre Yersin, seorang dokter Swiss/Perancis dan bakteriologis Institut Pasteur, pada saat epidemik plak di Hong Kong. Kitasato Shibasaburo, seorang bakteriologis Jepang yang belajar di Jerman juga menemukan agen plak. Namun, Yersin yang menyangkutkan plak dengan Y. pestis. Awalnya bakteri ini bernama Pasteurella pestis, namun diganti namanya pada 1967.
Setiap tahun, ribuan kasus plak masih dilaporkan ke WHO, namun dengan perawatan yang benar, prognosis korban lebih baik.
 Artikel utama untuk bagian ini adalah: Teori Kematian Hitam
Pada 2000, Didier Raoult dan rekan menemukan DNA Y. pestis setelah melakukan "PCR bunuh diri" pada organ pulp gigi dari kuburan plak abad ke-14 di Montpellier.
Artikel utama untuk bagian ini adalah: Teori Kematian Hitam
Pada 2000, Didier Raoult dan rekan menemukan DNA Y. pestis setelah melakukan "PCR bunuh diri" pada organ pulp gigi dari kuburan plak abad ke-14 di Montpellier.
Sebuah riset yang dilakukan oleh periset internasional pada Oktober 2010 mengkonfirmasi bahwa Y. pestis adalah penyebab Kematian Hitam dan epidemik berikutnya pada benua Eropa selama periode 400 tahun. Tim tersebut DNA kuno dan protein yang diambil dari jasad korban plak yang dikubur di Hereford, Inggris, di Saint-Laurent-de-la-Cabrerisse di Prancis, dan Bergen op Zoom di Belanda untuk mengidentifikasi patogen.
Walaupun terdapat 11 nama spesies dalam genus Yersinia, hanya tiga patogen yang dianggap penting bagi manusia:
Infeksi pada manusia mengambil tiga bentuk: pnumonik, septisemik, dan bubonik plak. Ketiga bentuk infeksi ini telah menyebabkan epidemik yang merenggut banyak korban dalah sejarah manusia, termasuk Plak Justinian pada 542 dan Kematian Hitam yang menyebabkan paling tidak mengambil sepertiga populasi Eropa dari 1347 sampai 1353. Belakangan ini, Y. Pestis juga dapat digunakan sebagai senjata biologi dan CDC telah mengklasifikasi bakteri ini ke dalam Patogen Kategori A sebagai persiapan serangan teroris.
Y. pestis ditemukan pada 1894 oleh Alexandre Yersin, seorang dokter Swiss/Perancis dan bakteriologis Institut Pasteur, pada saat epidemik plak di Hong Kong. Kitasato Shibasaburo, seorang bakteriologis Jepang yang belajar di Jerman juga menemukan agen plak. Namun, Yersin yang menyangkutkan plak dengan Y. pestis. Awalnya bakteri ini bernama Pasteurella pestis, namun diganti namanya pada 1967.
Setiap tahun, ribuan kasus plak masih dilaporkan ke WHO, namun dengan perawatan yang benar, prognosis korban lebih baik.
Peran dalam Kematian Hitam
Sebuah riset yang dilakukan oleh periset internasional pada Oktober 2010 mengkonfirmasi bahwa Y. pestis adalah penyebab Kematian Hitam dan epidemik berikutnya pada benua Eropa selama periode 400 tahun. Tim tersebut DNA kuno dan protein yang diambil dari jasad korban plak yang dikubur di Hereford, Inggris, di Saint-Laurent-de-la-Cabrerisse di Prancis, dan Bergen op Zoom di Belanda untuk mengidentifikasi patogen.
Keluarga Yersinia Pestis
Yersinia pestis sebelumnya telah diklasifikasikan dalam keluarga Pasteurellaceae, namun berdasarkan kesamaan dengan Escherichia coli (E. coli), maka Yersinia grup reclassified sebagai anggota dari keluarga Enterobacteriaceae.Walaupun terdapat 11 nama spesies dalam genus Yersinia, hanya tiga patogen yang dianggap penting bagi manusia:
- Yersinia pestis
- Yersinia pseudotuberculosis
- Yersinia enterocolitica.
Yersinia Pestis di Binatang
Yersinia pestis paling sering ditemukan pada tikus, tetapi kadang-kadang dalam hewan lainnya, seperti:- Tikus (Mice)
- Squirrels
- Kutu
- Kucing
- Anjing
- Tikus kayu
- Chipmunks.
Tularemia
Tularemia adalah penyakit menular yang disebabkan oleh bakteri Francisella tularensis. Penyakit ini didapat setelah bersentuhan dengan binatang dan unggas itu, oleh memakan daging yang tidak dimasak benar-benar dan dari gigitan kutu binatang atau serangga penghisap darah lain. Kelinci
ialah binatang sumber penyakit ini yang paling umum. Orang-orang yang
berisiko tinggi terhadap penyakit ini ialah para pemburu, tukang potong
hewan, dan ibu rumah tangga.
Daftar isi |
Penjangkitan
Kuman memasuki tubuh melalui luka pada kulit, melalui lapisan atau membran, atau oleh menelan atau menghisap kuman tersebut.Gejala
Gejala biasanya terjadi 3-7 hari sesudah kuman masuk. Ulkus atau luka terjadi pada membran atau kulit dengan pembengkakkan dan pecahnya kelenjar getah bening di daerah itu. Hal ini disertai panas tinggi, perasaan pusing yang berat, pembesaran hati dan limpa. Pada beberapa kasus, penyakit ini bisa menyerang paru-paru, alat-alat pencernaan, atau selaput mataTuberkulosis
Tuberkulosis atau TB (singkatan yang sekarang ditinggalkan adalah TBC) adalah penyakit infeksi yang disebabkan oleh bakteri Mycobacterium tuberculosis. Penyakit ini paling sering menyerang paru-paru walaupun pada sepertiga kasus menyerang organ
tubuh lain dan ditularkan orang ke orang. Ini juga salah satu penyakit
tertua yang diketahui menyerang manusia. Jika diterapi dengan benar
tuberkulosis yang disebabkan oleh kompleks Mycobacterium tuberculosis,
yang peka terhadap obat, praktis dapat disembuhkan. Tanpa terapi
tuberkulosa akan mengakibatkan kematian dalam lima tahun pertama pada
lebih dari setengah kasus.
Pada tahun 1992 WHO telah mencanangkan tuberkulosis sebagai Global Emergency. Laporan WHO tahun 2004 menyatakan bahwa terdapat 8,8 juta kasus baru tuberkulosis pada tahun 2002, sepertiga penduduk dunia telah terinfeksi kuman tuberkulosis dan menurut regional WHO jumlah terbesar kasus ini terjadi di Asia Tenggara yaitu 33% dari seluruh kasus di dunia.
Indonesia berada dalam peringkat ketiga terburuk di dunia untuk jumlah penderita TB. Setiap tahun muncul 500 ribu kasus baru dan lebih dari 140 ribu lainnya meninggal. Seratus tahun yang lalu, satu dari lima kematian di Amerika Serikat disebabkan oleh tuberkulosis.
Tuberkulosis masih merupakan penyakit infeksi saluran napas yang tersering di Indonesia. Keterlambatan dalam menegakkan diagnosa dan ketidakpatuhan dalam menjalani pengobatan mempunyai dampak yang besar karena pasien Tuberkulosis akan menularkan penyakitnya pada lingkungan,sehingga jumlah penderita semakin bertambah.
Pengobatan Tuberkulosis berlangsung cukup lama yaitu setidaknya 6 bulan pengobatan dan selanjutnya dievaluasi oleh dokter apakah perlu dilanjutkan atau berhenti, karena pengobatan yang cukup lama seringkali membuat pasien putus berobat atau menjalankan pengobatan secara tidak teratur, kedua hal ini ini fatal akibatnya yaitu pengobatan tidak berhasil dan kuman menjadi kebal disebut MDR ( multi drugs resistance ), kasus ini memerlukan biaya berlipat dan lebih sulit dalam pengobatannya sehingga diharapkan pasien disiplin dalam berobat setiap waktu demi pengentasan tuberkulosis di Indonesia
Tanggal 24 Maret diperingati dunia sebagai "Hari TBC" oleh sebab pada 24 Maret 1882 di Berlin, Jerman, Robert Koch mempresentasikan hasil studi mengenai penyebab tuberkulosis yang ditemukannya.
M.tuberculosis berbentuk batang, berukuran panjang 5µ dan lebar 3µ, tidak membentuk spora, dan termasuk bakteri aerob. Mycobacteria dapat diberi pewarnaan seperti bakteri lainnya, misalnya dengan Pewarnaan Gram. Namun, sekali mycobacteria diberi warna oleh pewarnaan gram, maka warna tersebut tidak dapat dihilangkan dengan asam. Oleh karena itu, maka mycobacteria disebut sebagai Basil Tahan Asam atau BTA. Beberapa mikroorganisme lain yang juga memiliki sifat tahan asam, yaitu spesies Nocardia, Rhodococcus, Legionella micdadei, dan protozoa Isospora dan Cryptosporidium. Pada dinding sel mycobacteria, lemak berhubungan dengan arabinogalaktan dan peptidoglikan di bawahnya. Struktur ini menurunkan permeabilitas dinding sel, sehingga mengurangi efektivitas dari antibiotik. Lipoarabinomannan, suatu molekul lain dalam dinding sel mycobacteria, berperan dalam interaksi antara inang dan patogen, menjadikan M. tuberculosis dapat bertahan hidup di dalam makrofaga.
Dalam memerangi penyebaran Tuberkulosis terutama pada anak anak yang masih rentan daya tahan tubuhnya maka pemerintah Indonesia telah memasukkan Imunisasi Tuberkulosis pada anak anak yang disebut sebagai Imunisasi BCG sebagai salah satu program prioritas imunisasi wajib nasional beserta dengan 4 jenis imunisasi wajib lainnya yaitu hepatitis B, Polio, DPT dan campak, jadwalnya ada di Jadwal imunisasi
Gejala klinis tuberkulosis dapat dibagi menjadi 2 golongan, yaitu gejala lokal dan gejala sistemik, bila organ yang terkena adalah paru maka gejala lokal ialah gejala respiratori atau gejala gejala yang erat hubungannya dengan organ pernapasan ( sedang gejala lokal lain akan sesuai dengan organ yang terlibat )
Gejala respiratori ialah batuk lebih dari 2 minggu, batuk bercampur darah. Bisa juga nyeri dada dan sesak napas. Selanjutnya ada gejala yang disebut sebagai Gejala sistemis antara lain Demam , badan lemah yang disebut sebagai malaise, keringat malam, anoreksia dan berat badan menurun menjadi semakin kurus. Gejala respiratori sangat bervariasi, dari mulai tidak ada gejala sampai gejala yang cukup berat tergantung dari luas lesi, sehingga pada kondisi yang gejalanya tidak jelas sehingga terkadang pasien baru mengetahui dirinya terdiagnosis Tuberkulosis saat medical check up
Pada tahun 1992 WHO telah mencanangkan tuberkulosis sebagai Global Emergency. Laporan WHO tahun 2004 menyatakan bahwa terdapat 8,8 juta kasus baru tuberkulosis pada tahun 2002, sepertiga penduduk dunia telah terinfeksi kuman tuberkulosis dan menurut regional WHO jumlah terbesar kasus ini terjadi di Asia Tenggara yaitu 33% dari seluruh kasus di dunia.
Indonesia berada dalam peringkat ketiga terburuk di dunia untuk jumlah penderita TB. Setiap tahun muncul 500 ribu kasus baru dan lebih dari 140 ribu lainnya meninggal. Seratus tahun yang lalu, satu dari lima kematian di Amerika Serikat disebabkan oleh tuberkulosis.
Tuberkulosis masih merupakan penyakit infeksi saluran napas yang tersering di Indonesia. Keterlambatan dalam menegakkan diagnosa dan ketidakpatuhan dalam menjalani pengobatan mempunyai dampak yang besar karena pasien Tuberkulosis akan menularkan penyakitnya pada lingkungan,sehingga jumlah penderita semakin bertambah.
Pengobatan Tuberkulosis berlangsung cukup lama yaitu setidaknya 6 bulan pengobatan dan selanjutnya dievaluasi oleh dokter apakah perlu dilanjutkan atau berhenti, karena pengobatan yang cukup lama seringkali membuat pasien putus berobat atau menjalankan pengobatan secara tidak teratur, kedua hal ini ini fatal akibatnya yaitu pengobatan tidak berhasil dan kuman menjadi kebal disebut MDR ( multi drugs resistance ), kasus ini memerlukan biaya berlipat dan lebih sulit dalam pengobatannya sehingga diharapkan pasien disiplin dalam berobat setiap waktu demi pengentasan tuberkulosis di Indonesia
Tanggal 24 Maret diperingati dunia sebagai "Hari TBC" oleh sebab pada 24 Maret 1882 di Berlin, Jerman, Robert Koch mempresentasikan hasil studi mengenai penyebab tuberkulosis yang ditemukannya.
Daftar isi |
Klasifikasi
- Tuberkulosis paru terkonfirmasi secara bakteriologis dan histologis
- Tuberkulosis paru tidak terkonfirmasi secara bakteriologis dan histologis
- Tuberkulosis pada sistem saraf
- Tuberkulosis pada organ-organ lainnya
- Tuberkulosis millier
Patofisiologi
Penyebab penyakit ini adalah bakteri kompleks Mycobacterium tuberculosis. Mycobacteria termasuk dalam famili Mycobacteriaceae dan termasuk dalam ordo Actinomycetales. kompleks Mycobacterium tuberculosis meliputi M. tuberculosis, M. bovis, M. africanum, M. microti, dan M. canettii. Dari beberapa kompleks tersebut, M. tuberculosis merupakan jenis yang terpenting dan paling sering dijumpai.M.tuberculosis berbentuk batang, berukuran panjang 5µ dan lebar 3µ, tidak membentuk spora, dan termasuk bakteri aerob. Mycobacteria dapat diberi pewarnaan seperti bakteri lainnya, misalnya dengan Pewarnaan Gram. Namun, sekali mycobacteria diberi warna oleh pewarnaan gram, maka warna tersebut tidak dapat dihilangkan dengan asam. Oleh karena itu, maka mycobacteria disebut sebagai Basil Tahan Asam atau BTA. Beberapa mikroorganisme lain yang juga memiliki sifat tahan asam, yaitu spesies Nocardia, Rhodococcus, Legionella micdadei, dan protozoa Isospora dan Cryptosporidium. Pada dinding sel mycobacteria, lemak berhubungan dengan arabinogalaktan dan peptidoglikan di bawahnya. Struktur ini menurunkan permeabilitas dinding sel, sehingga mengurangi efektivitas dari antibiotik. Lipoarabinomannan, suatu molekul lain dalam dinding sel mycobacteria, berperan dalam interaksi antara inang dan patogen, menjadikan M. tuberculosis dapat bertahan hidup di dalam makrofaga.
Penularan
Penularan penyakit ini karena kontak dengan dahak atau menghirup titik-titik air dari bersin atau batuk dari orang yang terinfeksi kuman tuberkulosis, anak anak sering mendapatkan penularan dari orang dewasa di sekitar rumah maupun saat berada di fasilitas umum seperti kendaraan umum, rumah sakit dan dari lingkungan sekitar rumah. Oleh sebab ini masyarakat di Indonesia perlu sadar bila dirinya terdiagnosis tuberkulosis maka hati hati saat berinteraksi dengan orang lain agar tidak batuk sembarangan , tidak membuang ludah sembarangan dan sangat dianjurkan untuk bersedia memakai masker atau setidaknya sapu tangan atau tissue.Dalam memerangi penyebaran Tuberkulosis terutama pada anak anak yang masih rentan daya tahan tubuhnya maka pemerintah Indonesia telah memasukkan Imunisasi Tuberkulosis pada anak anak yang disebut sebagai Imunisasi BCG sebagai salah satu program prioritas imunisasi wajib nasional beserta dengan 4 jenis imunisasi wajib lainnya yaitu hepatitis B, Polio, DPT dan campak, jadwalnya ada di Jadwal imunisasi
Diagnosis
Simtoma klinis
Diagnosa tuberkulosis dapat ditegakkan berdasarkan gejala klinis, pemeriksaan jasmani, pemeriksaan bakteriologi , radiologi dan pemeriksaan penunjang lainnyaGejala klinis tuberkulosis dapat dibagi menjadi 2 golongan, yaitu gejala lokal dan gejala sistemik, bila organ yang terkena adalah paru maka gejala lokal ialah gejala respiratori atau gejala gejala yang erat hubungannya dengan organ pernapasan ( sedang gejala lokal lain akan sesuai dengan organ yang terlibat )
Gejala respiratori ialah batuk lebih dari 2 minggu, batuk bercampur darah. Bisa juga nyeri dada dan sesak napas. Selanjutnya ada gejala yang disebut sebagai Gejala sistemis antara lain Demam , badan lemah yang disebut sebagai malaise, keringat malam, anoreksia dan berat badan menurun menjadi semakin kurus. Gejala respiratori sangat bervariasi, dari mulai tidak ada gejala sampai gejala yang cukup berat tergantung dari luas lesi, sehingga pada kondisi yang gejalanya tidak jelas sehingga terkadang pasien baru mengetahui dirinya terdiagnosis Tuberkulosis saat medical check up
Tetanus
Tetanus yang juga dikenal dengan lockjaw [1], merupakan penyakit yang disebakan oleh tetanospasmin, yaitu sejenis neurotoksin yang diproduksi oleh Clostridium tetani yang menginfeksi sistem urat saraf dan otot sehingga saraf dan otot menjadi kaku (rigid).[1] Kitasato merupakan orang pertama yang berhasil mengisolasi organisme dari korban manusia yang terkena tetanus dan juga melaporkan bahwa toksinnya dapat dinetralisasi dengan antibodi yang spesifik.[1] Kata tetanus diambil dari bahasa Yunani yaitu tetanos dari teinein yang berarti menegang.[2] Penyakit ini adalah penyakit infeksi di saat spasme otot tonik dan hiperrefleksia menyebabkan trismus (lockjaw), spasme otot umum, melengkungnya punggung (opistotonus), spasme glotal, kejang, dan paralisis pernapasan.[3]
Pada keadaan anaerobik, spora bakteri ini akan bergerminasi menjadi sel vegetatif.[3] Selanjutnya, toksin akan diproduksi dan menyebar ke seluruh bagian tubuh melalui peredaran darah dan sistem limpa.[3] Toksin tersebut akan beraktivitas pada tempat-tempat tertentu seperti pusat sistem saraf termasuk otak.[3] Gejala kronis yang ditimbulkan dari toksin tersebut adalah dengan memblok pelepasan dari neurotransmiter sehingga terjadi kontraksi otot yang tidak terkontrol.[3] Akibat dari tetanus adalah rigid paralysis (kehilangan kemampuan untuk bergerak) pada voluntary muscles (otot yang geraknya dapat dikontrol), sering disebut lockjaw karena biasanya pertama kali muncul pada otot rahang dan wajah.[8] Kematian biasanya disebabkan oleh kegagalan pernapasan dan rasio kematian sangatlah tinggi.[3]
Obat lainnya bisa diberikan untuk menenangkan penderita, mengendalikan kejang dan mengendurkan otot-otot.[7] Penderita biasanya dirawat di rumah sakit dan ditempatkan dalam ruangan yang tenang.[7] Untuk infeksi menengah sampai berat, mungkin perlu dipasang ventilator untuk membantu pernapasan.[7]
Makanan diberikan melalui infus atau selang nasogastrik.[9] Untuk membuang kotoran, dipasang kateter.[9] Penderita sebaiknya berbaring bergantian miring ke kiri atau ke kanan dan dipaksa untuk batuk guna mencegah terjadinya pneumonia.[9]
Untuk mengurangi nyeri diberikan kodein.[9] Obat lainnya bisa diberikan untuk mengendalikan tekanan darah dan denyut jantung. Setelah sembuh, harus diberikan vaksinasi lengkap karena infeksi tetanus tidak memberikan kekebalan terhadap infeksi berikutnya.
Pada seseorang yang memiliki luka, jika[10]:
Karakteristik Clostridium tetani
C. tetani termasuk dalam bakteri Gram positif, anaerob obligat, dapat membentuk spora, dan berbentuk drumstick.[4] Spora yang dibentuk oleh C. tetani ini sangat resisten terhadap panas dan antiseptik.[3] Ia dapat tahan walaupun telah diautoklaf (1210C, 10-15 menit) dan juga resisten terhadap fenol dan agen kimia lainnya.[3] Bakteri Clostridium tetani ini banyak ditemukan di tanah, kotoran manusia dan hewan peliharaan dan di daerah pertanian.[1][5] Umumnya, spora bakteri ini terdistribusi pada tanah dan saluran penceranaan serta feses dari kuda, domba, anjing, kucing, tikus, babi, dan ayam.[3] Ketika bakteri tersebut berada di dalam tubuh, ia akan menghasilkan neurotoksin (sejenis protein yang bertindak sebagai racun yang menyerang bagian sistem saraf).[1] C. tetani menghasilkan dua buah eksotoksin, yaitu tetanolysin dan tetanospasmin.[6] Fungsi dari tetanoysin tidak diketahui dengan pasti, namun juga dapat memengaruhi tetanus.[1] Tetanospasmin merupakan toksin yang cukup kuat.[6]Patogenesis dan Patofisiologi
Tetanus disebabkan neurotoksin (tetanospasmin) dari bakteri Gram positif anaerob, Clostridium tetani, dengan mula-mula 1 hingga 2 minggu setelah inokulasi bentuk spora ke dalam darah tubuh yang mengalami cedera (periode inkubasi).[4][7] Penyakit ini merupakan 1 dari 4 penyakit penting yang manifestasi klinis utamanya adalah hasil dari pengaruh kekuatan eksotoksin (tetanus, gas ganggren, dipteri, botulisme).[2] Tempat masuknya kuman penyakit ini bisa berupa luka yang dalam yang berhubungan dengan kerusakan jaringan lokal, tertanamnya benda asing atau sepsis dengan kontaminasi tanah, lecet yang dangkal dan kecil atau luka geser yang terkontaminasi tanah, trauma pada jari tangan atau jari kaki yang berhubungan dengan patah tulang jari dan luka pada pembedahan.[5]Pada keadaan anaerobik, spora bakteri ini akan bergerminasi menjadi sel vegetatif.[3] Selanjutnya, toksin akan diproduksi dan menyebar ke seluruh bagian tubuh melalui peredaran darah dan sistem limpa.[3] Toksin tersebut akan beraktivitas pada tempat-tempat tertentu seperti pusat sistem saraf termasuk otak.[3] Gejala kronis yang ditimbulkan dari toksin tersebut adalah dengan memblok pelepasan dari neurotransmiter sehingga terjadi kontraksi otot yang tidak terkontrol.[3] Akibat dari tetanus adalah rigid paralysis (kehilangan kemampuan untuk bergerak) pada voluntary muscles (otot yang geraknya dapat dikontrol), sering disebut lockjaw karena biasanya pertama kali muncul pada otot rahang dan wajah.[8] Kematian biasanya disebabkan oleh kegagalan pernapasan dan rasio kematian sangatlah tinggi.[3]
Pengobatan
Untuk menetralisir racun, diberikan immunoglobulin tetanus.[7] Antibiotik tetrasiklin dan penisilin diberikan untuk mencegah pembentukan racun lebih lanjut, supaya racun yang ada mati.[7]Obat lainnya bisa diberikan untuk menenangkan penderita, mengendalikan kejang dan mengendurkan otot-otot.[7] Penderita biasanya dirawat di rumah sakit dan ditempatkan dalam ruangan yang tenang.[7] Untuk infeksi menengah sampai berat, mungkin perlu dipasang ventilator untuk membantu pernapasan.[7]
Makanan diberikan melalui infus atau selang nasogastrik.[9] Untuk membuang kotoran, dipasang kateter.[9] Penderita sebaiknya berbaring bergantian miring ke kiri atau ke kanan dan dipaksa untuk batuk guna mencegah terjadinya pneumonia.[9]
Untuk mengurangi nyeri diberikan kodein.[9] Obat lainnya bisa diberikan untuk mengendalikan tekanan darah dan denyut jantung. Setelah sembuh, harus diberikan vaksinasi lengkap karena infeksi tetanus tidak memberikan kekebalan terhadap infeksi berikutnya.
Prognosis
Tetanus memiliki angka kematian sampai 50%.[2] Kematian biasanya terjadi pada penderita yang sangat muda, sangat tua dan pemakai obat suntik.[2] Jika gejalanya memburuk dengan segera atau jika pengobatan tertunda maka prognosisnya akan menjadi buruk.[2]Pencegahan
Mencegah tetanus melalui vaksinasi adalah jauh lebih baik daripada mengobatinya.[10] Pada anak-anak, vaksin tetanus diberikan sebagai bagian dari vaksin DPT (difteri, pertusis, tetanus).[10] Bagi yang sudah dewasa sebaiknya menerima booster.[10]Pada seseorang yang memiliki luka, jika[10]:
- Telah menerima booster tetanus dalam waktu 5 tahun terakhir, tidak perlu menjalani vaksinasi lebih lanjut
- Belum pernah menerima booster dalam waktu 5 tahun terakhir, segera diberikan vaksinasi
- Belum pernah menjalani vaksinasi atau vaksinasinya tidak lengkap, diberikan suntikan immunoglobulin tetanus dan suntikan pertama dari vaksinasi 3 bulanan.
Syankroid
Syankroid atau chancroid adalah penyakit menular seksual yang ditandai dengan rasa nyeri pada alat kelamin. Chancroid diketahui menyebar dari satu orang ke individu lainnya melalui hubungan seksual. Chancroid adalah infeksi bakteri yang disebabkan oleh Haemophilus ducreyi. Penyakit ini terutama ditemukan pada negara berkembang, berhubungan dengan pekerja seks komersial dan klien mereka.
Skarlatina
Penyakit Skarlatina atau juga dikenali sebagai Scarlet fever adalah satu penyakit berjangkit.
Masa inkubasi
Waktu terekspos sampai kena penyakit berbeda-beda (mungkin beberapa hari). Infeksi : 1 sampai 3 hari.Gejala
Sakit kerongkongan, demam tinggi dan muntah, diikuti dengan ruam dalam waktu 12 sampai 36 jam.Tempoh pengasingan yang disarankan
Ya, sampai sekurang-kurangnya 24 jam setelah perawatan telah mulai dan pesakit lebih sehat.Pencegahan
Mencuci tangan menggunakan air dan sabun dengan teliti. Orang dekat yang sakit harus bertemu dengan dokter mereka.Salmonelosis
Salmonelosis adalah infeksi akibat bakteri Salmonella. Kebanyakan orang yang terinfeksi salmonella mengalami diare, demam, muntah dan sakit perut
12 hingga 72 jam setelah infeksi. Dalam kebanyakan kasus, sakit
berlangsung 3 hingga 7 hari; kebanyakan orang yang terinfeksi dapat
pulih tanpa penanganan. Namun, pada beberapa orang, diare dapat sangat
parah sehingga patien menjadi dehidrasi dan harus dibawah ke rumah sakit.
Penyakit Rickettsia
Penyakit Rickettsia atau tifus adalah berbagai penyakit yang disebabkan oleh bakteri familia Rickettsiae.[1][2][3][4] Penyakit ini disebarkan oleh arthropoda, khususnya kutu, tungau, dan caplak.[2][3][4] Tiga jenis typhus utama adalah tifus epidemik, tifus endemik, dan tifus belukar.[2][4]
Jenis lain tifus yang juga sering ditemukan adalah penyakit
Brill-Zinsser, yang merupakan tifus epidemik yang muncul kembali setelah
bertahun-tahun sembuh.[5][4][2][6] Tifus epidemik dan penyakit Brill-Zinsser disebabkan oleh bakteri Rickettsia prowazekii.[4][2] Tifus epidemik disebarkan oleh kutu badan.[4][2] Tifus endemik disebabkan oleh bakteri Rickettsia typhi, yang disebarkan oleh kutu.[4][2] Tifus belukar disebabkan oleh bakteri Rickettsia tsutsugamushi (dahulu bernama Orientia tsutsugamushi), dan disebarkan oleh tungau dan caplak.[4][2][5][7] Jenis tifus lainnya antara lain demam berbintik gunung Rocky, Rickettsialpox, demam Boutonneuse, tifus caplak Siberia, tifus caplak Australia, dan demam berbintik Oriental.[5][8]

| Typhus | |
| Klasifikasi dan bahan-bahan eksternal | |
 |
|
|---|---|
| Rash caused by epidemic typhus | |
| ICD-10 | A75. |
| ICD-9 | 080-083 |
| DiseasesDB | 29240 |
| MedlinePlus | 001363 |
| eMedicine | med/2332 |
| MeSH | D014438 |

Penyemprotan insektisida DDT ke tubuh prajurit untuk membunuh arthropoda pembawa penyakit Rickettsia.
Pasteurella multocida
Pasteurella multocida adalah kokobasilus kecil, gram-negatif yang sensitif terhadap penisilin. Pasteurella multocida dapat menyebabkan infeksi zoonotik pada manusia, yang merupakan akibat dari gigitan atau cakaran dari binatang peliharaan (seperti kucing dan anjing).
Pasteurella multocida pertama kali ditemukan tahun 1878. Pasteurella multocida tidak diisolasi sampai tahun 1880, oleh Louis Pasteur - nama orang yang menjadi asal usul kata Pasteurella untuk menghormatinya.
Pasteurella multocida pertama kali ditemukan tahun 1878. Pasteurella multocida tidak diisolasi sampai tahun 1880, oleh Louis Pasteur - nama orang yang menjadi asal usul kata Pasteurella untuk menghormatinya.
mycobacterium avium complex
Mycobacterium avium adalah grup bakteri yang berhubungan dengan genetika dan masuk kedalam genus Mycobacterium. Mycobacterium avium subspecies avium (MAA), Mycobacterium avium subspecies hominis (MAH), dan Mycobacterium avium subspecies paratuberculosis (MAP) termasuk bagian dari genus ini.
Mycobacterium avium juga termasuk Mycobacterium avium intracellulare (spesies bakteri) secara sejarah.
Mycobacterium avium juga termasuk Mycobacterium avium intracellulare (spesies bakteri) secara sejarah.
Mikobakteria
| ?Mikobakterium | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
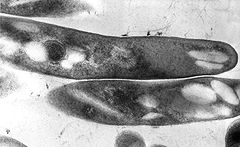 |
||||||||||||
| Klasifikasi ilmiah | ||||||||||||
|
||||||||||||
| Species | ||||||||||||
| See below. |
Meningokokus
Penyakit Meningokokus adalah satu penyakit
berjangkit. Neisseria menigitidis (meningokokus) merupakan bakteri
kokus gram negatif yang secara alami hidup di dalam tubuh manusis.
Meningokokus bisa menyebabkan infeksi pada selaput yang menyelimuti otak
dan sumsum tulang belakang (meningitis), infeksi darah dan infeksi
berat lainnya pada dewasa dan anak-anak. Neisseria gonorhoeae, juga
merupakan kokus gram negatif alami pada manusia, yang menyebabkan
gonore, suatu penyakit menular seksual yang bisa mengenai uretra, vagina
dan anus dan bisa menjalar ke sendi. Banyak spesies Neisseria yang
secara normal hidup di tenggorokan dan mulut, vagina dan usus, tetapi
mereka jarang menyebabkan infeksi.Neisseria menigitidis (meningokokus)
merupakan bakteri kokus gram negatif yang secara alami hidup di dalam
tubuh manusis. Meningokokus bisa menyebabkan infeksi pada selaput
pembungkus otak dan medulla spinalis (meningitis), infeksi darah dan
infeksi berat lainnya pada dewasa dan anak-anak.
Neisseria gonorhoeae, juga merupakan kokus gram negatif alami pada manusia, yang menyebabkan gonore, suatu penyakit menular seksual yang bisa mengenai uretra, vagina dan anus dan bisa menjalar ke sendi.
Banyak spesies Neisseria yang secara normal hidup di tenggorokan dan mulut, vagina dan usus, tetapi mereka jarang menyebabkan infeksi.
Neisseria gonorhoeae, juga merupakan kokus gram negatif alami pada manusia, yang menyebabkan gonore, suatu penyakit menular seksual yang bisa mengenai uretra, vagina dan anus dan bisa menjalar ke sendi.
Banyak spesies Neisseria yang secara normal hidup di tenggorokan dan mulut, vagina dan usus, tetapi mereka jarang menyebabkan infeksi.
Masa inkubasi
Waktu terekspos sampai kena penyakit 2 sampai 10 hari.Gejala
Demam mendadak dan kombinasi sakit kepala, leher pegal, mual, muntah, mengantuk dan ruam.Tempoh pengasingan yang disarankan
Dianjurkan memperoleh bantuan medis dengan segera. Pasien akan memerlukan perawatan di rumah sakit.Pencegahan
Jangan minum minuman yang sama. Orang yang dekat harus bertemu dengan dokter dengan segera jika gejala muncul, dan mungkin perlu minum antibiotik tertentu.Leptospirosis
| ?Leptospira[1] | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
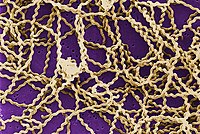
Bakteri Leptospira menggunakan Mikroskop elektron tipe scanning.
|
||||||||||||
| Klasifikasi ilmiah | ||||||||||||
|
||||||||||||
| Serovar[2] | ||||||||||||
|
Infeksi dalam bentuk subakut tidak begitu memperlihatkan gejala klinis, sedangkan pada infeksi akut ditandai dengan gejala sepsis, radang ginjal interstisial, anemia hemolitik, radang hati dan keguguran. [2]. Leptospirosis pada hewan biasanya subklinis [5]. Dalam keadaan ini, penderita tidak menunjukkan gejala klinis penyakit [5]. Leptospira bertahan dalam waktu yang lama di dalam ginjal hewan sehingga bakteri akan banyak dikeluarkan hewan lewat air kencingnya [5]. Leptospirosis pada hewan dapat terjadi berbulan-bulan sedangkan pada manusia hanya bertahan selama 60 hari[5]. Manusia merupakan induk semang terakhir sehingga penularan antarmanusia jarang terjadi. [5].
Sejarah Penyakit
Penyakit ini pertama kali dilaporkan pada tahun 1886 oleh Adolf Weil dengan gejala panas tinggi disertai beberapa gejala saraf serta pembesaran hati dan limpa. [6] Penyakit dengan gejala tersebut di atas oleh Goldsmith (1887) disebut sebagai Weil's Disease.[rujukan?] Pada tahun 1915 Inada berhasil membuktikan bahwa "Weil's Disease" disebabkan oleh bakteri Leptospira icterohemorrhagiae. [6]Etiologi
Bakteri penyebab Leptosirosis yaitu bakteri Leptospira sp. [3][7][5]. Bakteri Leptospira merupakan Spirochaeta aerobik (membutuhkan oksigen untuk bertahan hidup), motil (dapat bergerak), gram negatif, bentuknya dapat berkerut-kerut, dan terpilin dengan ketat [7]. Bakteri Lepstospira berukuran panjang 6-20 µm dan diameter 0,1-0,2 µm[3]. Sebagai pembanding, ukuran sel darah merah hanya 7 µm [7]. Jadi, ukuran bakteri ini relatif kecil dan panjang sehingga sulit terlihat bila menggunakan mikroskop cahaya dan untuk melihat bakteri ini diperlukan mikroskop dengan teknik kontras [7]. Bakteri ini dapat bergerak maju dan mundur [3].Leptospira mempunyai ±175 serovar [2], bahkan ada yang mengatakan Leptospira memiliki lebih dari 200 serovar [7]. Infeksi dapat disebabkan oleh satu atau lebih serovar sekaligus [2]. Bila infeksi terjadi, maka pada tubuh penderita dalam waktu 6-12 hari akan terbentuk zat kebal aglutinasi [3]. Leptospirosis pada anjing disebabkan oleh infeksi satu atau lebih serovar dari Leptospira interrogans [2]. Serovar yang telah diketahui dapat menyerang anjing yaitu L. australis, L. autumnalis, L. ballum, L. batislava, L. canicola, L. grippotyphosa, L. hardjo, L. ichterohemorarhagica, L. pomona, dan L. tarassovi [2][5]. Pada anjing, telah tersedia vaksin terhadap Leptospira yang mengandung biakan serovar L. canicola dan L. icterohemorrhagica yang telah dimatikan [2]. Serovar yang dapat menyerang sapi yaitu L. pamona dan L. gryptosa[5]. Serovar yang diketahui terdapat pada kucing adalah L. bratislava, L. canicola, L. gryppothyphosa, dan L. pomona [2]. Babi dapat terserang L. pamona dan L. interogans, sedangkan tikus dapat terserang L. ballum dan L. ichterohaemorhagicae [5].
Bila terkena bahan kimia atau dimakan oleh fagosit, bakteri dapat kolaps menjadi bola berbentuk kubah dan tipis [7]. Pada kondisi ini, Leptospira tidak memiliki aktifitas patogenik [7]. Leptospira dapat hidup dalam waktu lama di air, tanah yang lembap, tanaman dan lumpur.[8]
Distribusi Penyakit
Leptospirosis terjadi di seluruh dunia,[9] [8] baik di daerah pedesaan maupun perkotaan, di daerah tropis maupun subtropis [9]. Penyakit ini terutama beresiko terhadap orang yang bekerja di luar ruangan bersama hewan, misalnya peternak, petani, penjahit, dokter hewan, dan personel militer [9]. Selain itu, Leptospirosis juga beresiko terhadap individu yang terpapar air yang terkontaminasi [6][9]. Di daerah endemis, puncak kejadian Leptospirosis terutama terjadi pada saat musim hujan dan banjir.[9].Iklim yang sesuai untuk perkembangan Leptospira adalah udara yang hangat, tanah yang basah dan pH alkalis, kondisi ini banyak ditemukan di negara beriklim tropis.[6] Oleh sebab itu, kasus Leptospirosis 1000 kali lebih banyak ditemukan di negara beriklim tropis dibandingkan dengan negara subtropis dengan risiko penyakit yang lebih berat. [10]. Angka kejadian Leptospirosis di negara tropis basah 5-20/100.000 penduduk per tahun [11]. Organisasi Kesehatan Dunia (World Health Oraganization/WHO) mencatat, kasus Leptospirosis di daerah beriklim subtropis diperkirakan berjumlah 0.1-1 per 100.000 orang setiap tahun, sedangkan di daerah beriklim tropis kasus ini meningkat menjadi lebih dari 10 per 100.000 orang setiap tahun.[9] Pada saat wabah, sebanyak lebih dari 100 orang dari kelompok berisiko tinggi di antara 100.000 orang dapat terinfeksi.[9]
Di Indonesia, Leptospirosis tersebar antara lain di Provinsi Jawa Barat, Jawa Tengah, Daerah Istimewa Yogyakarta, Lampung, Sumatera Selatan, Bengkulu, Riau, Sumatera Barat, Sumatera Utara, Bali, NTB, Sulawesi Selatan, Sulawesi Utara, Kalimantan Timur dan Kalimantan Barat [12]. Angka kematian Leptospirosis di Indonesia termasuk tinggi, mencapai 2,5-16,45 persen [12]. Pada usia lebih dari 50 tahun kematian mencapai 56 persen [12]. Di beberapa publikasi angka kematian dilaporkan antara 3 persen - 54 persen tergantung sistem organ yang terinfeksi [13].
Cara Penularan
Leptospirosis merupakan penyakit yang dapat ditularkan melalui air (water borne disease)[9][3]. Urin (air kencing) dari individu yang terserang penyakit ini merupakan sumber utama penularan, baik pada manusia maupun pada hewan [5]. Kemampuan Leptospira untuk bergerak dengan cepat dalam air menjadi salah satu faktor penentu utama ia dapat menginfeksi induk semang (host) yang baru [7]. Hujan deras akan membantu penyebaran penyakit ini, terutama di daerah banjir [8]. Gerakan bakteri memang tidak memengaruhi kemampuannya untuk memasuki jaringan tubuh namun mendukung proses invasi dan penyebaran di dalam aliran darah induk semang [7].Di Indonesia, penularan paling sering terjadi melalui tikus pada kondisi banjir [14] [15]. Keadaan banjir menyebabkan adanya perubahan lingkungan seperti banyaknya genangan air, lingkungan menjadi becek, berlumpur, serta banyak timbunan sampah yang menyebabkan mudahnya bakteri Leptospira berkembang biak [15]. Air kencing tikus terbawa banjir kemudian masuk ke tubuh manusia melalui permukaan kulit yang terluka, selaput lendir mata dan hidung. [14]. Sejauh ini tikus merupakan reservoir dan sekaligus penyebar utama Leptospirosis [14] karena bertindak sebagai inang alami dan memiliki daya reproduksi tinggi [16]. Beberapa hewan lain seperti sapi, kambing, domba, kuda, babi, anjing dapat terserang Leptospirosis, tetapi potensi menularkan ke manusia tidak sebesar tikus [14].
Bentuk penularan Leptospira dapat terjadi secara langsung dari penderita ke penderita dan tidak langsung melalui suatu media [3][5]. Penularan langsung terjadi melalui kontak dengan selaput lendir (mukosa) mata (konjungtiva) [5], kontak luka di kulit, mulut, cairan urin [9], kontak seksual dan cairan abortus (gugur kandungan) [3]. Penularan dari manusia ke manusia jarang terjadi [9].
Penularan tidak langsung terjadi melalui kontak hewan atau manusia dengan barang-barang yang telah tercemar urin penderita, misalnya alas kandang hewan, tanah, makanan, minuman dan jaringan tubuh[5]. Kejadian Leptospirosis pada manusia banyak ditemukan pada pekerja pembersih selokan karena selokan banyak tercemar bakteri Leptospira[5]. Umumnya penularan lewat mulut dan tenggorokan sedikit ditemukan karena bakteri tidak tahan terhadap lingkungan asam [5].
Perjalanan Penyakit
Setelah bakteri Leptospira masuk ke dalam tubuh melalui kulit atau selaput lendir, maka bakteri akan mengalami multiplikasi (perbanyakan) di dalam darah dan jaringan [14]. Selanjutnya akan terjadi leptospiremia, yakni penimbunan bakteri Leptospira di dalam darah sehingga bakteri akan menyebar ke berbagai jaringan tubuh terutama ginjal dan hati [5].Di ginjal kuman akan migrasi ke interstitium, tubulus renal, dan tubular lumen menyebabkan nefritis interstitial (radang ginjal interstitial) dan nekrosis tubular (kematian tubuli ginjal) [5]. Gagal ginjal biasanya terjadi karena kerusakan tubulus, hipovolemia karena dehidrasi dan peningkatan permeabilitas kapiler [14]. Gangguan hati berupa nekrosis sentrilobular dengan proliferasi sel Kupffer [14]. Pada konsisi ini akan terjadi perbanyakan sel Kupffer dalam hati [5]. Leptospira juga dapat menginvasi otot skeletal menyebabkan edema, vakuolisasi miofibril, dan nekrosis fokal [14]. Gangguan sirkulasi mikro muskular dan peningkatan permeabilitas kapiler dapat menyebabkan kebocoran cairan dan hipovolemia sirkulasi [14].
Pada kasus berat akan menyebabkan kerusakan endotelium kapiler dan radang pada pembuluh darah [5]. Leptospira juga dapat menginvasi akuos humor mata dan menetap dalam beberapa bulan, sering mengakibatkan uveitis kronis dan berulang [14]. Setelah infeksi menyerang seekor hewan, meskipun hewan tersebut telah sembuh, biasaya dalam tubuhnya akan tetap menyimpan bakteri Leptospira di dalam ginjal atau organ reproduksinya untuk dikeluarkan dalam urin selama beberapa bulan bahkan tahun[5].
Gejala Klinis

Jaundis pada kucing: telinga dan mukosa mata menjadi kuning
Pada hewan
Pada hewan, Leptospirosis kadangkala tidak menunjukkan gejala klinis (bersifat subklinis), dalam arti hewan akan tetap terlihat sehat walaupun sebenarnya dia sudah terserang Leptospirosis [5]. Kucing yang terinfeksi biasanya tidak menunjukkan gejala walaupun ia mampu menyebarkan bakteri ini ke lingkungan untuk jangka waktu yang tidak pasti [2].Gejala klinis yang dapat tampak yaitu ikterus atau jaundis, yakni warna kekuningan, karena pecahnya butir darah merah (eritrosit) sehingga ada hemoglobin dalam urin [3]. Gejala ini terjadi pada 50 persen kasus, terutama jika penyababnya L. pomona [3]. Gejala lain yaitu demam, tidak nafsu makan, depresi, nyeri pada bagian-bagian tubuh [3], gagal ginjal, gangguan kesuburan, dan kadang kematian [5]. Apabila penyakit ini menyerang ginjal atau hati secara akut maka gejala yang timbul yaitu radang mukosa mata (konjungtivitis), radang hidung (rhinitis), radang tonsil (tonsillitis), batuk dan sesak napas [2].
Pada babi muncul gejala kelainan saraf, seperti berjalan kaku dan berputar-putar [3]. Pada anjing yang sembuh dari infeksi akut kadangkala tetap mengalami radang ginjal interstitial kronis atau radang hati (hepatitis) kronis [2]. Dalam keadaan demikian gejala yang muncul yaitu penimbunan cairan di abdomen (ascites), banyak minum, banyak urinasi, turun berat badan dan gejala saraf[2]. Pada sapi, infeksi Leptospirosis lebih parah dan lebih banyak terjadi pada pedet dibandingkan sapi dewasa dengan gejala demam, jaundis, anemia, warna telinga maupun hidung yang menjadi hitam, dan kematian (Bovine Leptospirosis).[17]. Angka kematian (mortalitas) akibat Leptospirosis pada hewan mencapai 5-15 persen, sedangkan angka kesakitannya (morbiditas) mencapai lebih dari 75 persen [3].
Pada Manusia
Masa inkubasi Leptospirosis pada manusia yaitu 2 - 26 hari [14]. Infeksi Leptospirosis mempunyai manifestasi yang sangat bervariasi dan kadang tanpa gejala, sehingga sering terjadi kesalahan diagnosa [14]. Infeksi L. interrogans dapat berupa infeksi subklinis yang ditandai dengan flu ringan sampai berat [18], Hampir 15-40 persen penderita terpapar infeksi tidak bergejala tetapi serologis positif [14]. Sekitar 90 persen penderita jaundis ringan, sedangkan 5-10 persen jaundis berat yang sering dikenal sebagai penyakit Weil [14]. Perjalanan penyakit Leptospira terdiri dari 2 fase, yaitu fase septisemik dan fase imun [14][5]. Pada periode peralihan fase selama 1-3 hari kondisi penderita membaik [14]. Selain itu ada Sindrom Weil yang merupakan bentuk infeksi Leptospirosis yang berat. [14]Fase Septisemik
Fase Septisemik dikenal sebagai fase awal atau fase leptospiremik karena bakteri dapat diisolasi dari darah, cairan serebrospinal dan sebagian besar jaringan tubuh [14]. Pada stadium ini, penderita akan mengalami gejala mirip flu selama 4-7 hari, ditandai dengan demam, kedinginan, dan kelemahan otot [5]. Gejala lain adalah sakit tenggorokan, batuk, nyeri dada, muntah darah, nyeri kepala, takut cahaya, gangguan mental, radang selaput otak (meningitis), serta pembesaran limpa dan hati [14].Fase Imun
Fase Imun sering disebut fase kedua atau leptospirurik karena sirkulasi antibodi dapat dideteksi dengan isolasi kuman dari urin, dan mungkin tidak dapat didapatkan lagi dari darah atau cairan serebrospinalis [14]. Fase ini terjadi pada 0-30 hari akibat respon pertahanan tubuh terhadap infeksi [14]. Gejala tergantung organ tubuh yang terganggu seperti selaput otak, hati, mata atau ginjal [14].Jika yang diserang adalah selaput otak, maka akan terjadi depresi, kecemasan, dan sakit kepala [5]. Pada pemeriksaan fungsi hati didapatkan jaundis, pembesaran hati (hepatomegali), dan tanda koagulopati [14]. Gangguan paru-paru berupa batuk, batuk darah, dan sulit bernapas.[5] Gangguan hematologi berupa peradarahan dan pembesaran limpa (splenomegali). Kelainan jantung ditandai gagal jantung atau perikarditis [14]. Meningitis aseptik merupakan manifestasi klinis paling penting pada fase imun [14].
Leptospirosis dapat diisolasi dari darah selama 24-48 jam setelah timbul jaundis [5]. Pada 30 persen pasien terjadi diare atau kesulitan buang air besar (konstipasi), muntah, lemah, dan kadang-kadang penurunan nafsu makan [5]. Kadang-kadang terjadi perdarahan di bawah kelopak mata dan gangguan ginjal pada 50 persen pasien, dan gangguan paru-paru pada 20-70 persen pasien [5].
Gejala juga ditentukan oleh serovar yang menginfeksi [14]. Sebanyak 83 persen penderita infeksi L. icterohaemorrhagiae mengalami ikterus, dan 30 persen pada L. pomona [14]. Infeksi L. grippotyphosa umumnya menyebabkan gangguan sistem pencernaan. Sedangkam L. pomona atau L. canicola sering menyebabkan radang selaput otak (meningitis) [14].
Sindrom Weil
Sindrom Weil adalah bentuk Leptospirosis berat ditandai jaundis, disfungsi ginjal, nekrosis hati, disfungsi paru-paru, dan diathesis perdarahan [5]. Kondisi ini terjadi pada akhir fase awal dan meningkat pada fase kedua, tetapi bisa memburuk setiap waktu [14]. Kriteria penyakit Weil tidak dapat didefinisikan dengan baik. Manifestasi paru meliputi batuk, kesulitan bernapas, nyeri dada, batuk darah, dan gagal napas [5]. Disfungsi ginjal dikaitkan dengan timbulnya jaundis 4-9 hari setelah gejala awal [14]. Penderita dengan jaundis berat lebih mudah terkena gagal ginjal, perdarahan dan kolap kardiovaskular. Kasus berat dengan gangguan hati dan ginjal mengakibatkan kematian sebesar 20-40 persen yang akan meningkat pada lanjut usia. [14]Diagnosa
Untuk mendiagnosa Leptospirosis, maka hal yang perlu diperhatikan adalah riwayat penyakit, gejala klinis dan diagnosa penunjang [5][19][14]. Sebagai diagnosa penunjang, antara lain dapat dilakukan pemeriksaan urin dan darah [19]. Pemeriksaan urin sangat bermanfaat untuk mendiagnosa Leptospirosis karena bakteri Leptospira terdapat dalam urin sejak awal penyakit dan akan menetap hingga minggu ketiga [19]. Cairan tubuh lainnya yang mengandung Leptospira adalah darah, serebrospinal [19] tetapi rentang peluang untuk isolasi bakteri sangat pendek [14]. Selain itu dapat dilakukan isolasi bakteri Leptospira dari jaringan lunak atau cairan tubuh penderita, misalnya jaringan hati, otot, kulit dan mata. Namun, isolasi Leptospira termasuk sulit dan membutuhkan waktu beberapa bulan [14].Untuk mengukuhkan diagnosa Leptospirosis biasanya dilakukan pemeriksaan serologis [19]. Antibodi dapat ditemukan di dalam darah pada hari ke-5-7 sesudah adanya gejala klinis [19]. Kultur atau pengamatan bakteri Leptospira di bawah mikroskop berlatar gelap umumnya tidak sensitif [19]. Tes serologis untuk mengkonfirmasi infeksi Leptospirosis yaitu Microscopic agglutination test (MAT) [5]. Tes ini mengukur kemampuan serum darah pasien untuk mengagglutinasi bakteri Leptospira yang hidup [18]. Namun, MAT tidak dapat digunakan secara spesifik pada kasus yang akut, yakni kasus yang terjadi secara cepat dengan gejala klinis yang parah [19]. Selain itu, diagnosa juga dapat dilakukan melalui pengamatan bakteri Leptospira pada spesimen organ yang terinfeksi menggunakan imunofloresen [19].
Pengobatan dan Pengendalian
Pada Hewan
Hewan, terutama hewan kesayangan, yang terinfeksi parah perlu diberikan perawatan intensif untuk menjamin kesehatan masyarakat dan mengoptimalkan perawatan.[20] Antibiotik yang dapat diberikan yaitu doksisiklin, enrofloksasin, ciprofloksasin atau kombinasi penisillin-streptomisin.[20] Selain itu diperlukan terapi suportif dengan pemberian antidiare, antimuntah, dan infus.[20]Pencegahan dapat dilakukan dengan memberikan vaksin Leptospira.[20][3] Vaksin Leptospira untuk hewan adalah vaksin inaktif dalam bentuk cair (bakterin) yang sekaligus bertindak sebagai pelarut karena umumnya vaksin Leptospira dikombinasikan dengan vaksin lainnya, misalnya distemper dan hepatitis.[3] Vaksin Leptospira pada anjing yang beredar di Indonesia terdiri atas dua macam serovar yaitu L. canicola dan L. ichterohemorrhagiae.[3] Vaksin Leptospira pada anjing diberikan saat anjing berumur 12 minggu dan diulang saat anjing berumur 14-16 minggu.[20] Sistem kekebalan sesudah vaksinasi bertahan selama 6 bulan, sehingga anjing perlu divaksin lagi setiap enam bulan.[20]
Pada Manusia
Leptospirosis yang ringan dapat diobati dengan antibiotik doksisiklin, ampisillin, atau amoksisillin. Sedangkan Leptospirosis yang berat dapat diobati dengan penisillin G, ampisillin, amoksisillin dan eritromisin.[5]Manusia rawan oleh infeksi semua serovar Leptospira sehingga manusia harus mewaspadai cemaran urin dari semua hewan.[5] Perilaku hidup sehat dan bersih merupakan cara utama untuk menanggulangi Leptospirosis tanpa biaya.[3] Manusia yang memelihara hewan kesayangan hendaknya selalu membersihkan diri dengan antiseptik setelah kontak dengan hewan kesayangan, kandang, maupun lingkungan di mana hewan berada.[5]
Manusia harus mewaspadai tikus sebagai pembawa utama dan alami penyakit ini.[6] Pemberantasan tikus terkait langsung dengan pemberantasan Leptospirosis.[15] Selain itu, para peternak babi dihimbau untuk mengandangkan ternaknya jauh dari sumber air.[3] Feses ternak perlu diarahkan ke suatu sumber khusus sehingga tidak mencemari lingkungan terutama sumber air.[3]
Langganan:
Komentar (Atom)





